Zakon ekvivalenata: formula i formulacija. Zakon o ekvivalentima kemije
Krajem XVIII. Stoljeća empirijski su dobiveni mnogi zakoni kemije. Mogu se koristiti i provoditi u praksi, ali točni su dokazi dobiveni tek mnogo desetljeća kasnije. Jedan od takvih stupova moderne kemije bio je zakon ekvivalenata, koji je izravno povezan s drugim temeljnim zakonima - zakonom o očuvanju mase i vladavinom višestrukih odnosa.
prapovijest
Temelj za novi položaj već je bio poznat krajem 18. stoljeća, zakonom stalnog sastava zakon o očuvanju mase. Zahvaljujući njemu, otkriveno je da različite kemikalije mogu međusobno djelovati ne proizvoljno, već u strogo određenim omjerima. Stoga se riječ "ekvivalentnost" pojavila u kemijskom leksikonu. Novi koncept u prijevodu na ruski znači "ekvivalentnost". To je bio prvi korak prema stvaranju pravila koje je kasnije postalo poznato kao zakon ekvivalenata. Brojni eksperimenti kasnije su opetovano potvrđivali teoretsku pretpostavku.
Novo pravilo
Zakon o ekvivalentima u kemiji nekoliko puta je promijenio njegovu formulaciju. U suvremenim udžbenicima piše se kako slijedi:
- "Ekvivalent bilo kojeg elementa smatra se takvom količinom koja se može povezati s jednim molom vodika."
Takva formulacija zakona ekvivalenata je univerzalna i koristi se u školskoj kemiji iu ozbiljnim znanstvenim eksperimentima. Na primjer, za poznati spoj, HCl, ekvivalent klora odgovara jednoj molitvi, a spojevima H2S, H20, ekvivalenti za sumpor i kisik će biti jednaki 1/2 mol, i tako dalje. U spojevima oblika Hn X, gdje je H vodik, X je drugi kemijski element, n je količina vodika u molekuli, ekvivalent elementa X uvijek će biti jednak 1 / n mol. Ovaj zakon ekvivalenta u kemiji proteže se na jednostavne tvari u kojima vodik stupa u interakciju s jednim elementom, te na spojeve u kojima je vodik susjedan mnogim drugim atomima.
Ekvivalentna masa
Zaključak novog zakona bio je novi koncept masa. Novi izraz je postao vrlo pogodan za mjerenje promjene tvari u reakcijama. Ekvivalentna masa se naziva masom od 1 ekvivalenta. Prema tome, zakon ekvivalenata predviđa masu drugog elementa čak i bez laboratorijskih istraživanja. U danom primjeru spoja klorovodične kiseline, ekvivalentna masa klora je 34,45 g / mol. U spoju H20, ekvivalentna masa kisika bit će 16: 2 = 8 g / mol, i tako dalje. 
Kako se to može izračunati
Ekvivalentna masa može se izračunati analizom dobivenih spojeva. Nije potrebno kombinirati s ispitivanom tvari s vodikom za izračunavanje ekvivalentne mase. Zakon ekvivalenta potvrđuje da je dovoljno poznavati sastav spoja određenog elementa i ekvivalentnu masu drugog elementa s kojim je povezan naš nepoznati uzorak. Primjer pronalaženja ekvivalenta je sljedeći zadatak:
Spoj 3 g natrija s viškom klora formira 7,62 g natrijevog klorida (natrijev klorid). Otkriti ekvivalentnu masu natrija, ako je eCl = 35,45 g / mol.
Iz uvjeta problema proizlazi da u produktu reakcije, kuhinjska sol, 3 g natrija iznosi 7,62 - 3 = 4,62 g klora. Otuda zaključak:
E Na = 3 x 35.45: 4,62 = 23 g / mol.
Molarna masa natrij se lako određuje iz periodnog sustava. Ona je jednaka 23 g / mol. Iz toga slijedi da je ekvivalentna masa natrija jednaka jednoj molitvi.
Teški elementi
Živa i neživa priroda koja nas okružuje sastoji se od mnogo različitih tvari, a većina njih je složena. Stoga se ekvivalenti često određuju drugačije, ovisno o sastavu iz kojeg susjednog spoja su izvedeni. Ali u svim proučavanim slučajevima, različiti ekvivalenti tretiraju jedni druge kao male cjeline. Na primjer, dovoljno je uzeti takve poznate spojeve kao oksid i sumporni dioksid. Ekvivalentne mase ovog elementa izračunate gore navedenom metodom daju vrijednosti od 16 g / mol i 32 g / mol. No, omjer tih vrijednosti sveden je na jednostavan oblik 1: 2.
To je pravilo empirijski izvedeno od poznatog engleskog kemičara, liječnika i prirodnjaka. Po Johnu Daltonu Samouki učitelj, koji je postavljao čudne pokuse, isprva je prestravio sluge i nasmijao susjede. Ipak, stavljajući svoje jednostavne pokuse, potvrdio je mnoge znanstvene pretpostavke. On je najprije formulirao zakon višestrukih odnosa.

Zakon ekvivalenta primjenjuje se na složene spojeve u kojima interagira nekoliko elemenata. Pojam ekvivalenta za jedan od elemenata u složenoj mješavini prestaje biti jednoznačan. Za takve spojeve, formulacija zakona ekvivalenata zvuči malo drugačije: "Kao ekvivalent kompleksne tvari, takva se količina koristi da sudjeluje u kemijskoj reakciji bez ostatka s jednim ekvivalentom elementa ili kompleksnog spoja, ili s jednim ekvivalentom vodika." 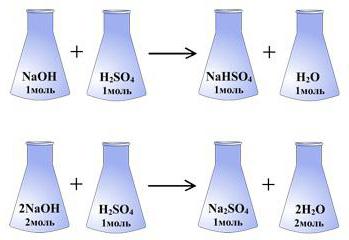
Ovo se pravilo koristi svugdje. Ako uklonite glomazne definicije, može se svesti na sljedeće: "Različite tvari mogu reagirati samo u količinama koje su proporcionalne njihovim ekvivalentima."
rješenja
U proučavanju i pripremi rješenja, svi gore navedeni zakoni su u potpunosti primjenjivi. Ovdje ulogu ekvivalenta igra nova jedinica, koja se naziva g / ekvivalent. To je ime količine tvari od kojih je jedna čestica (atom ili ion) kemijski ekvivalentna atomu ili vodikovom ionu. Dakle, zakon ekvivalenata za rješenja zvuči slično klasičnoj definiciji.

Opći zakon ekvivalenata
Formula za ekvivalente različitih spojeva općenito je sljedeća:
- E = molarna masa / (broj atoma elementa × valencija).
Kao što se može vidjeti, ekvivalentnost je izravno ovisna o molarnoj masi tvari i njezinoj valenciji. Ako kemičar ima informacije o ekvivalentima nepoznatih elemenata, može odrediti njegovu sposobnost ulaska u kemijske reakcije. Uz poznatu količinu grama / ekvivalenata tvari, znanstvenik može odmah napraviti zaključak o koncentraciji i svojstvima određene otopine.

stehiometrija
Kvantitativni sastav tvari i njihovi omjeri u spojevima posvećeni su zasebnom odjeljku kemije, nazvanom stehiometrija. Zadaci ovog dijela teorijske kemije su izračunati kvantitativne odnose u spojevima. Za jednostavne tvari to je vrlo jednostavno, a za složene tvari, proteine ili viruse stehiometrijski izračuni postaju vrlo težak zadatak.