Amonijeve soli: svojstva. Amonijeve soli: primjena
Amonij je jedan od mnogih dušikovih spojeva. Njegove soli imaju niz zanimljivih svojstava i pronalaze praktičnu primjenu u mnogim područjima ljudske aktivnosti. Proučavanje svojstava ovog elementa bavi se kemijom. Amonijeve soli proučavaju se u proučavanju interakcije dušika s drugim kemijskim elementima. 
Što je amonij
Da biste saznali što je amonij, trebali biste se bolje upoznati s načelom kombiniranja atoma dušika i ugljika. Molekula amonijaka zapisana je u obliku NH3. Atom dušika je vezan kovalentnim vezama na tri protona. Zbog unutarnje strukture dušika, jedna veza ostaje neraspoređena. 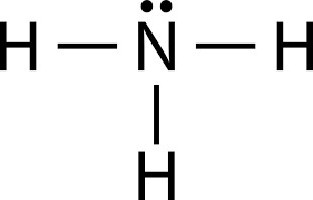
Stoga NH3 aktivno ulazi u različite kovalentne veze s drugim elementima, koristeći nedodijeljeni par elektrona. Ako jezgra vodika uđe u spoj, nastaje amonijev ion. Shema reakcije je prikazana ispod: 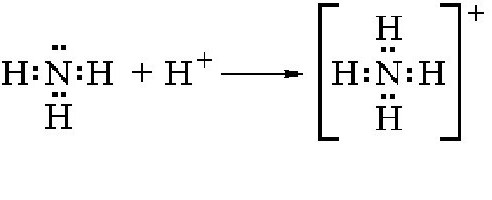
Kao što možete vidjeti, u ovoj reakciji, molekula amonijaka je akceptor jednog protona i tako se ponaša kao baza. Amonij ne postoji u svom slobodnom obliku, jer se gotovo trenutno raspada u vodik i amonijak. Amonijeve soli dobivaju se kao rezultat interakcije ovog elementa s drugim tvarima. Kao što pokazuju praktični eksperimenti, amonij ulazi u različite spojeve s kiselinama, neutralizirajući ih i tvoreći amonijeve soli. Na primjer, u slučaju reakcije klorovodična kiselina nastaje jedna od soli ovog elementa:
NH3 + HCl = NH4C1
Rezultat reakcije je solni klorid amonij.
Interakcija vode
Amonijak dobro reagira s vodom. Kao rezultat reakcije dobivaju se amonijačni hidrati s povećanom koncentracijom OH - . Zapis o kemijskoj reakciji:
NH3 + H20 → NH4 + OH -
Budući da je broj iona hidroksokrupe iznimno velik, vodene otopine amonijaka imaju alkalnu reakciju. Međutim, prema staroj kemijskoj navici, vodena otopina amonijaka je zabilježena kao NH4OH. Ova tvar se naziva amonijev hidroksid, a alkalna reakcija ovog spoja smatra se disocijacijom molekula u koje se razgrađuje amonijak.
Amonijeve soli. Svojstva i glavne značajke
Većina soli NH4 je praktički bezbojna i prilično topljiva u vodi. Ovaj spoj ima mnoga svojstva metala, stoga se amonijeve soli ponašaju na isti način kao i soli različitih metala. Evo nekoliko primjera ove sličnosti:
- NH 4 soli su dobri elektroliti. Oni se podvrgavaju hidrolizi u različitim otopinama. Ova reakcija se može pratiti na primjeru disocijacije amonijevog klorida:
NH4C1 = NH4 + HCl -
- Podvrgnuti hidrolizi. Rezultat je reakcija soli slabe baze i jaka kiselina :
- imaju ionsku kristalnu rešetku, imaju električnu provodljivost;
- ne održavati visoke temperature i razbijati se na komponente.
Nepovratni i reverzibilni procesi
Razgradnja amonijevih soli pod utjecajem temperature može biti ireverzibilna, ili može biti reverzibilni proces. Ako anion soli pokazuje slaba svojstva oksidatora, sol se razgrađuje reverzibilno. Klasični amonijev klorid je klasičan primjer takve reakcije: s povećanjem temperature reakcije na kraju se razlaže na vlastite izvorne elemente - klorovodik, kao i amonijak. Ako se zidovi posude ne zagrijavaju, na njima se pojavljuje napad. Tako nastaje amonijev klorid. 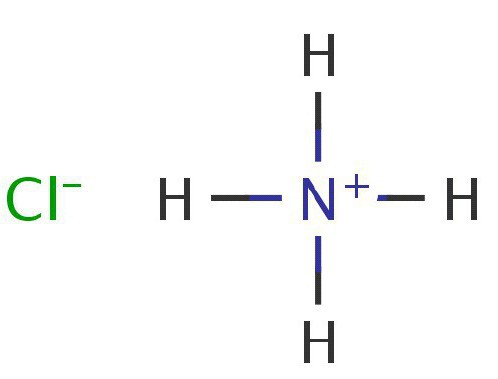
Ostale soli ovog elementa, u kojima anion ima izražena oksidirajuća svojstva, nepovratno se raspadaju. Standardni primjer takve reakcije je razgradnja amonijevog nitrata, koja je kako slijedi:
NH4NO3 = N20 + H20
Kako jedan od produkata interakcije napušta svoje polje, reakcija se zaustavlja.
Upotreba amonijaka i amonijevih soli
Značajan udio amonijaka, industrijski izvađen, odnosi se na njegovu uporabu u postrojenjima za zamrzavanje i hlađenje. Amonijeve soli koriste se u svakodnevnom životu iu medicini. Ali velika većina amonijaka ide u proizvodnju dušična kiselina i razne spojeve koji sadrže dušik, prvenstveno različita mineralna gnojiva.
Dušična gnojiva
Najpoznatije soli derivata dušika, čija je uporaba u gospodarskim djelatnostima izuzetno važna - to je amonijev sulfat, amonijev nitrat, amonijev klorid. Dušik je neophodna komponenta proteina. Taj je element obvezan za postojanje bilo kojeg živog organizma. Biljke izvlače dušik iz plodnog tla, gdje je taj element uglavnom vezan. Dušik se obično nalazi kao amonijeve soli i spojevi dušične kiseline. Rastvarajući se u vlažnom tlu, ti anorganski spojevi ulaze u biljne organizme i prerađuju ih u različite proteine i aminokiseline. Životinje i ljudi ne mogu apsorbirati dušik u slobodnom obliku ili kao jednostavni spojevi. Za prehranu i rast potrebni su proteini, čija je komponenta nužno dušik. Samo uz sudjelovanje biljaka dobivamo element koji nam je potreban za život i zdravlje.  Tla u prirodnom okruženju sadrže malu količinu dušika. Nakon žetve svakog usjeva, mala količina dušika koja se prethodno nalazila u zemljištu se prenosi zajedno s biljkama. Ubrzati proces regeneracije tla i primijeniti dušična gnojiva.
Tla u prirodnom okruženju sadrže malu količinu dušika. Nakon žetve svakog usjeva, mala količina dušika koja se prethodno nalazila u zemljištu se prenosi zajedno s biljkama. Ubrzati proces regeneracije tla i primijeniti dušična gnojiva.
Amonijev sulfat. Formula za ovaj spoj je (NH4) 2 SO 4. Ova amonijeva sol tvori osnovu za mnoštvo gnojiva.
Amonijev nitrat. Formula za ovu tvar je NH4NO3. Također je dobro poznato gnojivo koje biljke dobro apsorbiraju. Osim u poljoprivredne svrhe, amonijev nitrat se koristi u vojnoj i rudarskoj industriji - na njemu se rade od eksplozivnih smjesa (amonijak), koje se koriste za miniranje. 
nišador
Amonijev klorid. Dobro poznat kao amonijak. Njegova kemijska formula je NH 4 Cl. Ovaj spoj je dobro poznat u proizvodnji boja i lakova, u tekstilnoj industriji, amonijak se koristi u galvanskim stanicama. Amonijev klorid dobro je poznat dioničarima i rudarima. U svom radu često koriste soli amonijevog klorida. Upotreba ove tvari pomaže pri uklanjanju najtanjeg filma oksida s površine metala. Dodir zagrijanog metala amonijaku uzrokuje odgovarajuću reakciju oksida - oni ili odlaze na kloride ili se smanjuju. Kloridi brzo isparavaju s metalne površine. Postupak reakcije bakra može se napisati na sljedeći način:
4CuO + 2NH4C1 = 3Cu + 2CuCl2 + N2 + 4H20.
Amonijak u tekućem obliku i jake otopine amonijevih soli također se koriste kao dušična gnojiva - sadržaj dušika u njima je viši nego u čvrstim gnojivima, a biljke ih bolje apsorbira.