Octena kiselina: kemijska formula, svojstva i primjena
Etanoična kiselina je bolje poznata kao octena kiselina. Ona predstavlja organski spoj sa formulom CH3COOH. Spada u klasu karboksilnih kiselina, čije molekule sadrže funkcionalne monovalentne karboksilne skupine COOH (jednu ili više). O tome možete pružiti puno informacija, ali sada pozornost treba istaknuti samo najzanimljivije činjenice.
formula
Kako to izgleda, može se razumjeti na slici ispod. Kemijska formula octene kiseline nije jednostavna. To je posljedica mnogih: sam spoj je monobazičan i pripada karboksilnoj skupini koja je karakterizirana lakim protonskim cijepanjem (stabilna elementarna čestica). Ovaj spoj je tipičan predstavnik karboksilnih kiselina, budući da ima sva njihova svojstva.
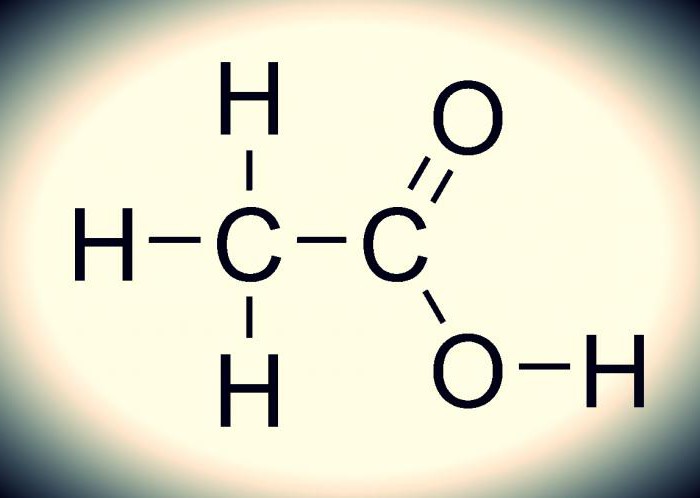
Veza između kisika i vodika (-COOH) je visoko polarna. To uzrokuje jednostavan proces disocijacije (otapanja, razgradnje) ovih spojeva i manifestacije njihovih kiselinskih svojstava.
Kao rezultat, formiraju se proton H + i acetatni ion CH3COO. Koje su to tvari? Acetatni ion je ligand povezan s određenim akceptorom (objekt koji prima nešto od spoja donora), formirajući stabilne acetatne komplekse s kationima mnogih metala. I proton je, kao što je gore spomenuto, čestica sposobna za hvatanje elektrona iz elektrona M-, K- ili L- ljuske atoma.
Kvalitativna analiza
Temelji se upravo na disocijaciji octene kiseline. Kvalitativna analiza, također nazvana reakcija, je kombinacija fizikalnih i kemijskih metoda koje se koriste za otkrivanje spojeva, radikala (neovisnih molekula i atoma) i elemenata (kombinacija čestica) koji čine analit.
Pomoću ove metode moguće je detektirati soli octene kiseline. Sve izgleda ne tako teško kao što se čini. U otopinu se dodaje jaka kiseline. sumporna, na primjer. A ako postoji miris octene kiseline, onda je njegova sol prisutna u otopini. Kako to funkcionira? Ostaci octene kiseline, koji se formiraju iz soli, vezani su u tom trenutku s vodikovim kationima iz sumporne kiseline. Što je rezultat? Pojava većeg broja molekula octene kiseline. Došlo je do disocijacije.
reakcija
Treba napomenuti da je spoj o kojem se raspravlja sposoban za interakciju s aktivnim metalima. To uključuje litij, natrij, kalij, rubidij, francij, magnezij, cezij. Potonji je, naime, najaktivniji. Što se događa u vrijeme takvih reakcija? Vodik se razvija, a nastaje i ozloglašeni acetat. Ovdje je kemijska formula octene kiseline koja reagira s magnezijem: Mg + 2CH3COOH → (CH3COO) 2 Mg + H2.

Postoje načini za dobivanje dikloroctene (CHCl2COOH) i trikloroctene (CCl3COOH) kiseline. U njima su vodikovi atomi metil grupe zamijenjeni klornim. Postoje samo dva načina da se to postigne. Jedan je hidroliza trikloretilena. I to je rjeđe od drugih, na temelju sposobnosti octene kiseline da se klorira djelovanjem plinovitog klora. Ova metoda je jednostavnija i učinkovitija.
Evo kako ovaj proces izgleda kao kemijska formula octene kiseline koja interagira s klorom: CH3COOH + Cl2 → CH2CLCOOH + HCl. Jedino je vrijedno razjasniti jednu stvar: to je jednostavno klorooctena kiselina, dva navedena gore su formirana uz sudjelovanje crvenog fosfora u malim količinama.
Ostale transformacije
Vrijedi napomenuti da octena kiselina (CH3COOH) može ući u sve reakcije koje su karakteristične za ozloglašenu karboksilnu skupinu. Može se vratiti u etanol, monohidrični alkohol. Da bi se to postiglo, potrebno je djelovati na njega s litij aluminij hidridom, anorganskim spojem koji je snažan redukcijski agens koji se često koristi u organskoj sintezi. Njegova formula je Li (AlH4).

Octena kiselina se također može pretvoriti u kiseli klorid, aktivni agens za aciliranje. To se događa pod utjecajem tionil klorida. Usput, to je klorid sumporne kiseline. Njegova formula je H2S03. Također je vrijedno spomenuti da je natrijeva sol octene kiseline dekarboksilirana kada je zagrijana s alkalijama (isključena je molekula ugljikovog dioksida), zbog čega nastaje metan (CH2). A on je, kao što znate, najjednostavniji ugljikovodik, koji je lakši od zraka.
kristalizacija
Ledena octena kiselina - često se taj spoj naziva tako. Činjenica je da kada se ohladi na samo 15-16 ° C, prelazi u kristalno stanje, kao da se smrzava. Vizualno, ovo je vrlo slično ledu. Ako postoji nekoliko sastojaka, možete provesti eksperiment, a rezultat toga bit će pretvorba octene kiseline u led. Jednostavno je. Iz vode i leda morate pripremiti rashladnu smjesu, a zatim spustiti prethodno pripremljenu cijev s octenom kiselinom. Nakon nekoliko minuta kristalizira. Osim spoja, potrebna je i čaša, stativ, termometar i epruveta.
Štetna tvar
Octena kiselina, čija je kemijska formula i svojstva navedena gore, nije sigurna. Njezini parovi iritiraju sluznice gornjih dišnih putova. Prag za percepciju mirisa ovog spoja u zraku je oko 0,4 mg / l. No, tu je i koncept maksimalno dopuštene koncentracije - sanitarni i higijenski standard, odobren zakonom. Prema njegovim riječima, u zraku može biti i do 0,06 mg / m³ ove tvari. A kada je riječ o radnim prostorijama, granica se povećava na 5 mg / m 3 .

Razarajuće djelovanje kiseline na biološka tkiva izravno ovisi o razrijedenosti vode. Najopasnija rješenja s sadržajem ove tvari više od 30%. A ako osoba slučajno dođe u kontakt s koncentriranim spojem, neće moći izbjeći kemijske opekline. To kategorički ne može biti dopušteno, jer se nakon te koagulacijske nekroze počinje razvijati - smrt bioloških tkiva. Smrtonosna doza je samo 20 ml.
efekti
Logično je da što je veća koncentracija octene kiseline, to će više štetiti u slučaju dodira s kožom ili u tijelo. Uobičajeni simptomi trovanja uključuju:
- Acidoza. Kislinsko-bazna ravnoteža pomaknuta je prema povećanoj kiselosti.
- Krvni ugrušci i njihovo zgrušavanje.
- Hemoliza eritrocita, njihovo uništavanje.
- Oštećenje jetre.
- Hemoglobinuria. U mokraći se pojavljuje hemoglobin.
- Akutno zatajenje bubrega.
- Toksični opekleni šok.
Stupnjevi ozbiljnosti
Uobičajeno je izdvojiti tri:
- Jednostavno. Karakteriziraju ga male opekline jednjaka i usta. Ali nema zgrušavanja krvi, a unutarnji organi i dalje normalno funkcioniraju.
- Prosječni. Postoji trovanje, šok i zadebljanje krvi. To utječe na želudac.
- Teški. Gornji dišni putovi, zidovi probavnog trakta su ozbiljno pogođeni, a dolazi do zatajenja bubrega. Maksimalni bolni šok. Možda razvoj opeklina.

Moguće je i trovanje parom octene kiseline. Prati ga ozbiljan curenje iz nosa, kašljanje i kidanje.
pomoći
Ako je osoba otrovana octenom kiselinom, vrlo je važno brzo djelovati kako bi se smanjile posljedice onoga što se dogodilo. Razmotrite što učiniti:
- Isperite usta. Ne gutajte vodu.
- Napravite ispiranje želuca. Potrebno je 8-10 litara hladne vode. Čak ni primjesa krvi nije kontraindikacija. Jer u prvim satima trovanja veliki brodovi i dalje ostaju netaknuti. Dakle, neće biti opasnog krvarenja. Prije pranja analgetici trebaju biti analgetici. Sonda je podmazana vazelinskim uljem.
- Ne izazivajte povraćanje! Neutralizirati tvar može biti spaljena magnezija ili lijek "Almagel".
- Ništa od navedenog? Zatim žrtva dobiva led i suncokretovo ulje - trebate uzeti nekoliko gutljaja.
- Dopuštena je uporaba pogođene smjese mlijeka i jaja.
Važno je pružiti prvu pomoć u roku od dva sata nakon incidenta. Nakon tog perioda, sluznice se nabubre i bit će teško smanjiti bol osobe. I da, ni u kojem slučaju ne mogu koristiti soda. Kombinacija kiseline i lužine dat će reakciju tijekom koje će se razviti ugljični dioksid i vode. I takva formacija u želucu može biti fatalna.
primjena
Vodene otopine etanonske kiseline naširoko se koriste u prehrambenoj industriji. To su octa. Da bi se dobila, kiselina se razrijedi s vodom da se dobije 3-15% otopina. Kao aditiv označeni su s E260. Ocat je dio raznih umaka, a koristi se i za konzerviranje proizvoda, konzerviranje mesa i riba. U svakodnevnom životu, oni su široko primjenjivi za uklanjanje kamenca, mrlja od odjeće i pribora. Ocat je izvrstan dezinficijens. Mogu podnijeti bilo koju površinu. Ponekad se dodaje prilikom pranja za omekšavanje odjeće.

Primjenjuje se i ocat u pripremi mirisnih tvari, lijekova, otapala, primjerice u proizvodnji acetona i celuloznog acetata. Da, i octena kiselina je izravno uključena u bojenje i tipografiju.
Osim toga, koristi se kao reakcijski medij za oksidaciju raznih organskih tvari. Primjer iz industrije je oksidacija para-ksilena (aromatskog ugljikovodika) atmosferskim kisikom u tereftalnu aromatsku kiselinu. Usput, budući da pare ove tvari imaju oštar iritantan miris, može se koristiti kao zamjena za amonijak za uklanjanje osobe iz nesvjestice.
Sintetska octena kiselina
To je zapaljiva tekućina koja spada u supstance treće vrste opasnosti. Koristi se u industriji. Prilikom rada s njim koristi se osobna zaštitna oprema. Čuvajte ovu tvar u posebnim uvjetima i samo u određenom spremniku. Obično je to:
- čiste željezničke cisterne;
- kontejnera;
- cisterne, bačve, spremnici od nehrđajućeg čelika (kapacitet do 275 dm 3 );
- staklene boce;
- polietilenske bačve kapaciteta do 50 dm3;
- zatvoreni spremnici od nehrđajućeg čelika.

Ako je tekućina pohranjena u polimernoj posudi, onda je to najviše mjesec dana. Također, kategorički nije dopušteno pohranjivanje ove tvari zajedno s takvim jakim oksidacijskim sredstvima kao što su kalijev permanganat, sumporna i dušična kiselina.
Sastav octa
O njemu bi također trebalo reći nekoliko riječi. Sastav tradicionalnog, uobičajenog octa uključuje sljedeće kiseline:
- Malić. Formula: NOORSN-CH (HE) COOH. Radi se o uobičajenom dodatku hrani (E296) prirodnog podrijetla. Sadrži nezrele jabuke, maline, planinski jasen, žuticu i grožđe. U duhanu i duhanu je prikazan u obliku nikotinskih soli.
- Mliječni. Formula: CH2CH (OH) COOH. Stvoren tijekom razgradnje glukoze. Dodatak hrani (E270), koji se dobiva mliječnom fermentacijom.
- Askorbinska. Formula: C2H204. Dodatak hrani (E300), koji se koristi kao antioksidans koji sprječava oksidaciju proizvoda.
I naravno, etanski spoj je također uključen u ocat - to je osnova ovog proizvoda.
Kako razrijediti?
Ovo je često postavljano pitanje. Svi su vidjeli prodaju 70% octene kiseline. Kupuje se kako bi se pripremile mješavine za popularni tretman, ili za upotrebu kao začina, marinada, aditiv u umaku ili uvaljivanje. Ali ne možete koristiti tako moćan koncentrat. Stoga se postavlja pitanje kako razrijediti octenu kiselinu do octa. Prvo se morate zaštititi - nosite rukavice. Tada treba pripremiti čistu vodu. Za otopine različitih koncentracija bit će potrebna određena količina tekućine. Koji Pa pogledajte tablicu ispod i razrijedite octenu kiselinu s obzirom na podatke.
Koncentracija octa | Početna koncentracija octa 70% |
30 | 1: 1,5 (omjer je jedan dio octa do n-tog dijela vode) |
10 | 1: 6 |
9 | 1: 7 |
8 | 1: 8 |
7 | 1: 9 |
6 | 01:11 |
5 | 01:13 |
4 | 01:17 |
3 | 01:22 |
U principu, ništa komplicirano. Da biste dobili 9% otopinu, trebate uzeti količinu vode u mililitrima koristeći ovu formulu: 100 grama octa pomnoženo s početnom brzinom (70%) i podijeljeno s 9. Što se događa? Brojka je 778. Iz ovoga se oduzima 100, budući da je izvorno uzeto 100 grama kiseline. Ispada 668 mililitara vode. Ta se količina pomiješa sa 100 g octa. Rezultat je cijela boca od 9 posto otopine.
Iako, možete se ponašati još lakše. Mnogi su zainteresirani za proizvodnju octa iz octene kiseline. Jednostavno! Glavno je zapamtiti da je za jedan dio 70% otopine potrebno uzeti 7 dijelova vode.